Разделы сайта
Выбор редакции:
- Уральские рабочие в армии колчака
- Профильные смены в детских лагерях
- История римской империи от начала до конца кратко, годы существования, интересные факты
- Модель Вселеной. Стационарная Вселенная. Размер вселенной Космологическая модель ранней вселенной эра излучения
- Царь — колокол и его плохая карма — интересные факты
- «Очарованный странник Краткое содержание очарованный странник
- Значение слова биосинтез Новый толково-словообразовательный словарь русского языка, Т
- Поэзия бодлера. Бодлер шарль пьер. Стихи и музыка
- Как решать математические ребусы
- Расписание уроков шаблон для заполнения в ворде
Реклама
| Химические свойства карбоновых кислот и методы получения. Карбоновые кислоты: физические свойства |
|
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп. Число карбоксильных групп характеризует основность кислоты. В зависимости от количества карбоксильных групп карбоновые кислоты подразделяются на одноосновные карбоновые кислоты (содержат одну карбоксильную группу), двухосновные (содержат две карбоксильные группы) и многоосновные кислоты. В зависимости от вида радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные, непредельные и ароматические. Предельные и непредельные кислоты объединяют под общим названием кислоты алифатического или жирного ряда.
1.1 Гомологический ряд и номенклатураГомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты Формула гомологического ряда Номенклатура ИЮПАК разрешает сохранять для многих кислот их тривиальные названия, которые обычно указывают на природный источник, из которого была выделена та или иная кислота, например, муравьиная, уксусная, масляная, валериановая и т.д. Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н-СООН называется метановой кислотой, уксусная кислота СН 3 -СООН - этановой кислотой и т. д. Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:
При составлении названий кислот с разветвленной цепью по рациональной номенклатуре их рассматривают как производные уксусной кислоты, в молекуле которой атомы водорода замещены радикалами, например, триметилуксусная кислота (СН 3) 3 С – СООН. 1.2 Физические свойства карбоновых кислотТолько с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства. Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:
Следствием этого является значительное ослабление связи О-Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н +). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С-С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты. Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами: Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты - 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью. Для большинства одноосновных карбоновых кислот рК а = 4,8, только муравьиная кислота имеет меньшую величину рК а (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп. В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:
Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:
Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона. Первые четыре представителя ряда карбоновых кислот - подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), - маслянистые жидкости, растворимость их в воде невелика. Высшие кислоты (от С 10) - твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются. Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.
На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты образуют прочные водородные связи, так как связи О-Н в них сильно поляризованы. Кроме того, карбоновые кислоты способны образовывать водородные связи с участием атома кислорода карбонильного диполя, обладающего значительной электроотрицательностью. Действительно, в твердом и жидком состоянии карбоновые кислоты существуют в основном в виде циклических димеров: Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях. Классификацияа) По основности (т. е. числукарбоксильных групп в молекуле): Одноосновные (монокарбоновые) RCOOH; например: СН 3 СН 2 СН 2 СООН; НООС-СН 2 -СООН пропандиовая (малоновая) кислота  Трехосновные (трикарбоновые) R(COOH) 3 и т. д. б) По строению углеводородного радикала: Алифатические предельные; например: СН 3 СН 2 СООН; непредельные; например: СН 2 =СНСООН пропеновая(акриловая) кислота  Алициклические, например:  Ароматические, например:  Предельные монокарбоновые кислоты(одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой -COOH. Все они имеют общую формулу C n H 2n+1 COOH (n ≥ 0); или CnH 2n O 2 (n≥1) НоменклатураСистематические названия одноосновных предельных карбоновых кислот даются по названию соответствующего алкана с добавлением суффикса - овая и слова кислота. 1. НСООН метановая (муравьиная) кислота 2. СН 3 СООН этановая (уксусная) кислота 3. СН 3 СН 2 СООН пропановая (пропионовая) кислота ИзомерияИзомерия скелета в углеводородном радикале проявляется, начиная с бутановой кислоты, которая имеет два изомера:  Межклассовая изомерия проявляется, начиная с уксусной кислоты: CH 3 -COOH уксусная кислота; H-COO-CH 3 метилформиат (метиловый эфир муравьиной кислоты); HO-CH 2 -COH гидроксиэтаналь (гидроксиуксусный альдегид); HO-CHO-CH 2 гидроксиэтиленоксид. Гомологический ряд
Кислотные остатки и кислотные радикалы
Электронное строение молекул карбоновых кислот
Показанное в формуле смещение электронной плотности в сторону карбонильного атома кислорода обусловливает сильную поляризацию связи О-Н, в результате чего облегчается отрыв атома водорода в виде протона - в водных растворах происходит процесс кислотной диссоциации: RCOOH ↔ RCOO - + Н + В карбоксилат-ионе (RCOO -) имеет место р, π-сопряжение неподеленной пары электронов атома кислорода гидроксильной группы с р-облаками, образующими π- связь, в результате происходит делокализация π- связи и равномерное распределение отрицательного заряда между двумя атомами кислорода:
В связи с этим для карбоновых кислот, в отличие от альдегидов, не характерны реакции присоединения. Физические свойства
Температуры кипения кислот значительно выше температур кипения спиртов и альдегидов с тем же числом атомов углерода, что объясняется образованием циклических и линейных ассоциатов между молекулами кислот за счет водородных связей: Химические свойстваI. Кислотные свойстваСила кислот уменьшается в ряду: НСООН → СН 3 СООН → C 2 H 6 COOH → ... 1. Реакции нейтрализацииСН 3 СООН + КОН → СН 3 СООК + н 2 O 2. Реакции с основными оксидами2HCOOH + СаО → (НСОО) 2 Са + Н 2 O 3. Реакции с металлами2СН 3 СН 2 СООН + 2Na → 2СН 3 СН 2 COONa + H 2 4. Реакции с солями более слабых кислот (в т. ч. с карбонатами и гидрокарбонатами)2СН 3 СООН + Na 2 CO 3 → 2CH 3 COONa + CO 2 + Н 2 O 2НСООН + Mg(HCO 3) 2 → (НСОО) 2 Мg + 2СO 2 + 2Н 2 O (НСООН + НСО 3 - → НСОО - + СO2 +Н2O) 5. Реакции с аммиакомСН 3 СООН + NH 3 → CH 3 COONH 4 II. Замещение группы -ОН1. Взаимодействие со спиртами (реакции этерификации) 2. Взаимодействие с NH 3 при нагревании (образуются амиды кислот) Амиды кислот  или их солей:  3. Образование галогенангидридовНаибольшее значение имеют хлорангидриды. Хлорирующие реагенты - PCl 3 , PCl 5 , тионилхлорид SOCl 2 .  4. Образование ангидридов кислот (межмолекулярная дегидратация) Ангидриды кислот образуются также при взаимодействии хлорангидридов кислот с безводными солями карбоновых кислот; при этом можно получать смешанные ангидриды различных кислот; например:  III. Реакции замещения атомов водорода у α-углеродного атома  Особенности строения и свойств муравьиной кислотыСтроение молекулы Молекула муравьиной кислоты, в отличие от других карбоновых кислот, содержит в своей структуре альдегидную группу. Химические свойстваМуравьиная кислота вступает в реакции, характерные как для кислот, так и для альдегидов. Проявляя свойства альдегида, она легко окисляется до угольной кислоты: В частности, НСООН окисляется аммиачным раствором Ag 2 O и гидроксидом меди (II) Сu(ОН) 2 , т. е. дает качественные реакции на альдегидную группу:  При нагревании с концентрированной H 2 SO 4 муравьиная кислота разлагается на оксид углерода (II) и воду:  Муравьиная кислота заметно сильнее других алифатических кислот, так как карбоксильная группа в ней связана с атомом водорода, а не с электроно-донорным алкильным радикалом. Способы получения предельных монокарбоновых кислот1. Окисление спиртов и альдегидовОбщая схема окисления спиртов и альдегидов: В качестве окислителей используют KMnO 4 , K 2 Cr 2 O 7 , HNO 3 и другие реагенты. Например: 5С 2 Н 5 ОН + 4KMnO 4 + 6H 2 S0 4 → 5СН 3 СООН + 2K 2 SO 4 + 4MnSO 4 + 11Н 2 O 2. Гидролиз сложных эфиров 3. Окислительное расщепление двойных и тройных связей в алкенах и в алкинах Способы получения НСООН (специфические)1. Взаимодействие оксида углерода (II) с гидроксидом натрияСO + NaOH → HCOONa формиат натрия 2HCOONa + H 2 SO 4 → 2НСООН + Na 2 SO 4 2. Декарбоксилирование щавелевой кислоты Способы получения СН 3 СООН (специфические)1. Каталитическое окисление бутана 2. Синтез из ацетилена 3. Каталитическое карбонилирование метанола 4. Уксуснокислое брожение этанолаТак получают пищевую уксусную кислоту. Получение высших карбоновых кислотГидролиз природных жиров Непредельные монокарбоновые кислотыВажнейшие представителиОбщая формула алкеновых кислот: C n H 2n-1 COOH (n ≥ 2) CH 2 =CH-COOH пропеновая (акриловая) кислота  Высшие непредельные кислотыРадикалы этих кислот входят в состав растительных масел. C 17 H 33 COOH - олеиновая кислота, или цис -октадиен-9-овая кислота
Транс -изомер олеиновой кислоты называется элаидиновой кислотой. C 17 H 31 COOH - линолевая кислота, или цис, цис -октадиен-9,12-овая кислота  C 17 H 29 COOH - линоленовая кислота, или цис, цис, цис -октадекатриен-9,12,15-овая кислота Кроме общих свойств карбоновых кислот, для непредельных кислот характерны реакции присоединения по кратным связям в углеводородном радикале. Так, непредельные кислоты, как и алкены, гидрируются и обесцвечивают бромную воду, например:  Отдельные представители дикарбоновых кислотПредельные дикарбоновые кислоты HOOC-R-COOHHOOC-CH 2 -COOH пропандиовая (малоновая) кислота, (соли и эфиры - малонаты) HOOC-(CH 2) 2 -COOH бутадиовая (янтарная) кислота, (соли и эфиры - сукцинаты) HOOC-(CH 2) 3 -COOH пентадиовая (глутаровая) кислота, (соли и эфиры - глутораты) HOOC-(CH 2) 4 -COOH гексадиовая (адипиновая) кислота, (соли и эфиры - адипинаты) Особенности химических свойствДикарбоновые кислоты во многом сходны с монокарбоновыми, однако являются более сильными. Например, щавелевая кислотасильнее уксусной почти в 200 раз. Дикарбоновые кислоты ведут себя как двухосновные и образуют два ряда солей - кислые и средние: HOOC-COOH + NaOH → HOOC-COONa + H 2 O HOOC-COOH + 2NaOH → NaOOC-COONa + 2H 2 O При нагревании щавелевая и малоновая кислоты легко декарбоксилируются: 
Способы получения . 1 . Окисление альдегидов и первичных спиртов - общий способ получения карбоновых кислот. В качестве окислителей применяются />K М n О 4 и K 2 С r 2 О 7 . 2 Другой общий способ - гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода - такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:/>
3 . Получение карбоновых кислот из цианидов (нитрилов) - это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия, например:/> СН 3 -В r + NaCN → CH 3 — CN + NaBr . Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония: CH 3 CN + 2Н 2 О → CH 3 COONH 4 . При подкислении раствора выделяется кислота: CH 3 COONH 4 + HCl → СН 3 СООН + NH 4 Cl . 4 . Использование реактива Гриньяра по схеме:/> Н 2 О 5 . Гидролиз сложных эфиров:/> R — COOR 1 + КОН → R — COOK + R ‘ OH , R — COOK + HCl → R — COOH + KCl . 6 . Гидролиз ангидридов кислот:/> (RCO ) 2 O + Н 2 О → 2 RCOOH . 7 . Для отдельных кислот существуют специфические способы получения./> Муравьиную кислоту получают нагреванием оксида углерода (II ) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой: Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха: 2С 4 Н 10 + 5 O 2 → 4СН 3 СООН + 2Н 2 О. Для получения бензойной кислоты можно использовать окисление монозамешенных гомологов бензола кислым раствором перманганата калия: 5С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5С 6 Н 5 СООН + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O . Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Канниццаро . В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенилметанола (бензилового спирта): Химические свойства . Карбоновые кислоты - более сильные кислоты, чем спирты, поскольку атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:/> RCOOH
Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты - это, как правило, слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой диссоциации К а = 1,7*10 -5 . /> Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта . Такие заместители, как хлор или фенильный радикал оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект (-/). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, +I. Они понижают кислотность. Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях констант диссоциации K a для ряда кислот. Кроме того, на силу кислоты оказывает влияние наличие сопряженной кратной связи.
Взаимное влияние атомов в молекулах дикарбоновых кислот приводит к тому, что они являются более сильными, чем одноосновные. 2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот: 2 RCOOH + М g → (RCOO ) 2 Mg + Н 2 , 2 RCOOH + СаО → (RCOO ) 2 Ca + Н 2 О, RCOOH + NaOH → RCOONa + Н 2 О, RCOOH + NaHCO 3 → RCOONa + Н 2 О + СО 2 . Карбоновые кислоты - слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей: CH 3 COONa + HCl → СН 3 СООН + NaCl . Соли карбоновых кислот в водных растворах гидролизованы: СН 3 СООК + Н 2 О
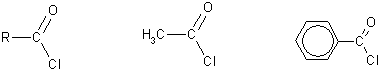
Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных. 3 . Образование функциональных производных карбоновых кислот. При замещении группы ОН в карбоновых кислотах различными группами (/>X ) образуются функциональные производные кислот, имеющие общую формулу R -СО- X ; здесь R означает алкильную либо арильную группу. Хотя нитрилы имеют другую общую формулу (R - CN ), обычно их также рассматривают как производные карбоновых кислот, поскольку они могут быть получены из этих кислот. Хлорангидриды получают действием хлорида фосфора (V ) на кислоты: R-CO-OH + РС l 5 → R-CO-Cl + РОС l 3 + HCl .
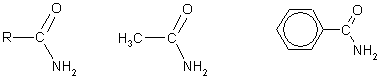
Ангидриды образуются из карбоновых кислот при действии водоотнимающих средств: 2 R — CO — OH + Р 2 О 5 → (R — CO -) 2 O + 2НРО 3 . Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации): Механизм реакции этерификации был установлен методом "меченых атомов". Сложные эфиры можно также получить при взаимодействии хлорангидридов кислот и алкоголятов щелочных металлов: R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl . Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов : СН 3 -СО-С l + CН 3 → СН 3 -СО-CН 2 + HCl . Кроме того, амиды могут быть получены при нагревании аммонийных солей карбоновых кислот: При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов :
Функциональные производные низших кислот — летучие жидкости. Все они легко гидролизуются с образованием исходной кислоты: R-CO-X + Н 2 О →R-CO-OH + НХ . В кислой среде эти реакции могут быть обратимы. Гидролиз в щелочной среде необратим и приводит к образованию солей карбоновых кислот, например: R-CO-OR ‘ + NaOH → R-CO-ONa + R’OH. 4 . Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода (а-атоме):/>
Непредельные карбоновые кислоты способны к реакциям присоединения: СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН, СН 2 =СН-СООН + С l 2 → СН 2 С l -СНС l -СООН, СН 2 =СН-СООН + HCl → СН 2 С l -СН 2 -СООН, СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН, Две последние реакции протекают против правила Марковникова. Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации .
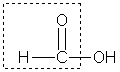
5 . Окислительно-восстановительные реакции карбоновых кислот./> Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды: Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:
Муравьиная кислота - сильный восстановитель и легко окисляется до СО 2 . Она дает реакцию "серебряного зеркала" : НСООН + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O, или в упрощенном виде: C Н 3 НСООН + Аg 2 О → 2Аg + СО 2 + Н 2 О. Кроме того, муравьиная кислота окисляется хлором: НСООН + Сl 2 → СО 2 + 2 HCl . В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О: СН 3 СООН + 2О 2 → 2СО 2 + 2Н 2 О. 6 . Реакции декарбоксширования . Насыщенные незамещенные монокарбоновые кислоты из-за большой прочности связи С-С при нагревании декарбоксилируются с трудом. Для этого необходимо сплавление соли щелочного металла карбоновой кислоты со щелочью:/> Появление электронодонорных заместителей в углеводородном радикале способствует реакции декарбоксилирования : Двухосновные карбоновые кислоты легко отщепляют СО 2 при нагревании: Химические соединения, основу которых составляет одна и более групп СООН, получили определение карбоновые кислоты. В основу соединений входит группа СООН, имеющая два составляющих — карбонил и гидроксил. Группу атомов СООН называют карбоксильной группой (карбоксилом). Взаимодействие элементов обеспечивается сочетанием двух атомов кислорода и атома углерода. Вконтакте Строение карбоновых кислотУглеводородный радикал в одноосновных предельных кислотах соединяется с одной группой СООН. Общая формула карбоновых кислот выглядит так: R-COOH. Строение карбоновой группы влияет на химические свойства. НоменклатураВ названии карбоновых соединений сначала нумеруют атом углерода группы COOH. Количество карбоксильных групп обозначают приставками ди-; три-; тетра-. Например,СН3-СН2-СООН — формула пропановой кислоты. У карбоновых соединений существуют и привычные слуху названия: муравьиная, уксусная, лимонная…Все это названия карбоновых кислот. Названия солей карбоновых соединений получаются из названий углеводорода с добавлением суффикса «-оат» (СООК)2- этандиот калия. Классификация карбоновых кислотКарбоновые кислоты классификация . По характеру углеводорода:
По количеству групп СООН бывают:
Предельные карбоновые кислоты — соединения, в которых радикал соединен с одним карбонилом. Классификация карбоновых кислот разделяет их еще и по строению радикала, с которым связан карбонил. По этому признаку соединения бывают алифатические и алициклические. Физические свойства
Карбоновые соединения имеют различное число атомов углерода. В зависимости от этого числа физические свойства этих соединений различаются. Соединения, имеющие в составе от одного до трех углеродных атомов, считаются низшими. Это жидкости без цвета с резким запахом. Низшие соединения с легкостью растворяются в воде. Соединения, имеющие в составе от четырех до девяти углеродных атомов — маслянистые жидкости, имеющие неприятный запах. Соединения, имеющие в составе более девяти углеродных атомов, считаются высшими и физические свойства этих соединений таковы: они являются твердыми веществами , их невозможно растворить в воде. Температура кипения и плавления зависит от молекулярной массы вещества. Чем больше молекулярная масса, тем выше температура кипения. Для закипания и плавления нужна более высокая температура, чем спиртам. Существует несколько способов получения карбоновых кислот . 
При химических реакциях проявляются следующие свойства:  Применение карбоновых кислотКарбоновые соединения распространены в природе.Поэтому их применяют во многих областях: в промышленности (легкой и тяжелой), в медицине и сельском хозяйстве , а также в пищевой промышленности и косметологии. Ароматические в большом количестве содержатся в ягодах и фруктах. В медицине используют молочную, винную и аскорбиновую кислоту. Молочную применяют в качестве прижигания, а винную — как легкое слабительное. Аскорбиновая укрепляет иммунитет.
Высокомолекулярные непредельные соединения встречаются в диетологии. Олеиновая в этой области наиболее распространена. Полиненасыщенные с двойными связями (линолевая и другие) обладают биологической активностью. Их еще называют активными жирными кислотами. Они участвуют в обмене веществ, влияют на зрительную функцию и иммунитет, а также на нервную систему. Отсутствие этих веществ в пище или недостаточное их употребление затормаживает рост животных и оказывает негативное влияние на их репродуктивную функцию. Сорбиновая получается из ягод рябины. Она является отличным консервантом . Акриловая имеет едкий запах. Она применяется для получения стекла и синтетических волокон. На основе реакции этирификации происходит синтез жира, который применяют при изготовлении мыла, а также моющих средств. Муравьиная используется в медицине , в пчеловодстве, а также в качестве консервантов. Уксусная — жидкость без цвета с резким запахом; легко смешивается с водой. Ее широко применяют в пищевой промышленности в качестве приправы. Также она используется при консервации. Еще она обладает свойствами растворителя. Поэтому широко применяется в производстве лаков и красок, при крашении. На ее основе изготавливают сырье для борьбы с насекомыми и сорняками. Стеариновая и пальмитиновая (высшие одноосновные соединения) являются твердыми веществами и не растворяются в воде. Но их соли применяются в производстве мыла. Они делают брикеты мыла твердыми. Поскольку соединения способны придавать однородность массам, то они широко используются в изготовлении лекарств. Растения и животные также вырабатывают карбоновые соединения. Поэтому употреблять их внутрь безопасно. Главное, — соблюдать дозировку. Превышение дозы и концентрации ведет к ожогам и отравлениям. Едкость соединений приносит пользу в металлургии, а также реставраторам и мебельщикам. Смеси на их основе позволяют выравнивать поверхности и очищать ржавчину. Сложные эфиры, получаемые при реакции этерификации, нашли свое применение в парфюмерии. Они используются также в качестве компонентов лаков и красок, растворителей. А также как аромадобавки.
Химические соединения, которые состоят в том числе и из карбоксильной группы COOH, получили от ученых название карбоновые кислоты. Существует большое количество наименований этих соединений. Они классифицируются по разным параметрам, например, по количеству функциональных групп, наличию ароматического кольца и так далее. Строение карбоновых кислотКак уже упоминалось, для того чтобы кислота была карбоновой, она должна иметь карбоксильную группу, которая, в свою очередь, имеет две функциональные части: гидроксил и карбонил. Их взаимодействие обеспечивается ее функциональным сочетанием одного атома углерода с двумя кислородными. Химические свойства карбоновых кислот зависят от того, какое строение имеет эта группа. За счет карбоксильной группы эти органические соединения можно называть кислотами. Их свойства обуславливаются повышенной способностью иона водорода H+ притягиваться к кислороду, дополнительно поляризуя связь O-H. Также благодаря этому свойству органические кислоты способны диссоциировать в водных растворах. Способность к растворению уменьшается обратно пропорционально росту молекулярной массы кислоты. Разновидности карбоновых кислотХимики выделяют несколько групп органических кислот. Моноосновные карбоновые кислоты состоят из углеродного скелета и только одной функциональной карбоксильной группы. Каждый школьник знает химические свойства карбоновых кислот. 10 класс учебной программы по химии включает в себя непосредственно изучение свойств одноосновных кислот. Двухосновные и многоосновные кислоты имеют в своей структуре две и более карбоксильных групп соответственно.
Также по наличию или отсутствию двойных и тройных связей в молекуле бывают ненасыщенные и насыщенные карбоновые кислоты. Химические свойства и их отличия будут рассмотрены ниже. Если органическая кислота имеет в составе радикала замещенный атом, то в ее название включается наименование группы-заместителя. Так, если атом водорода замещен галогеном, то в названии кислоты будет присутствовать наименование галогена. Такие же изменения претерпит наименование, если произойдет замещение на альдегидную, гидроксильную или аминогруппы. Изомерия органических карбоновых кислотВ основе получения мыла лежит реакция синтеза сложных эфиров вышеперечисленных кислот с калиевой или натриевой солью. Способы получения карбоновых кислотСпособов и методов получения кислот с группой COOH существует множество, но наиболее часто применяются следующие:
Значение карбоновых кислот для человека и промышленности
Химические свойства карбоновых кислот имеют большое значение для жизнедеятельности человека. Они чрезвычайно необходимы для организма, так как в большом количестве содержатся в каждой клетке. Метаболизм жиров, белков и углеводов всегда проходит через стадию, на которой получается та или иная карбоновая кислота. Кроме того, карбоновые кислоты используют при создании лекарственных препаратов. Ни одна фармацевтическая промышленность не может существовать без применения на деле свойств органических кислот.
Немаловажную роль соединения с карбоксильной группой играют и в косметической промышленности. Синтез жира для последующего изготовления мыла, моющих средств и бытовой химии основан на реакции этерификации с карбоновой кислотой. Химические свойства карбоновых кислот находят отражение в жизнедеятельности человека. Они имеют большое значение для человеческого организма, так как в большом количестве содержатся в каждой клетке. Метаболизм жиров, белков и углеводов всегда проходит через стадию, на которой получается та или иная карбоновая кислота. |
| Читайте: |
|---|
Популярное:
Новое
- Профильные смены в детских лагерях
- История римской империи от начала до конца кратко, годы существования, интересные факты
- Модель Вселеной. Стационарная Вселенная. Размер вселенной Космологическая модель ранней вселенной эра излучения
- Царь — колокол и его плохая карма — интересные факты
- «Очарованный странник Краткое содержание очарованный странник
- Значение слова биосинтез Новый толково-словообразовательный словарь русского языка, Т
- Поэзия бодлера. Бодлер шарль пьер. Стихи и музыка
- Как решать математические ребусы
- Расписание уроков шаблон для заполнения в ворде
- Евгений Евтушенко - биография, личная жизнь, жёны, дети поэта


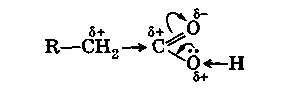







 гидролизуются с образованием кислот:
гидролизуются с образованием кислот:

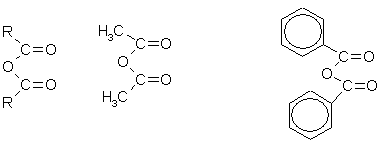

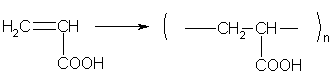
 Рассмотрим карбоновые кислоты физические свойства.
Рассмотрим карбоновые кислоты физические свойства. В косметологии используются фруктовые и ароматические. Благодаря им клетки быстрее обновляются. Аромат цитрусовых способен оказать тонизирующее и успокаивающее действие на организм. Бензойная встречается в бальзамах и эфирных маслах, она хорошо растворяется в спирте.
В косметологии используются фруктовые и ароматические. Благодаря им клетки быстрее обновляются. Аромат цитрусовых способен оказать тонизирующее и успокаивающее действие на организм. Бензойная встречается в бальзамах и эфирных маслах, она хорошо растворяется в спирте.